11kl_rudzitis_feldman_gdz Chimie 2018
Când uleiul este produs etilena cracare. Care este cel mai simplu aminoacid poate fi sintetizat din ea? Asigurați ecuația reacțiilor corespunzătoare.
Acesta poate fi sintetizat aminoetanovuyu (acid aminoacetic, glicină) de etilenă în modul următor: apa aderare la etilenă, în prezența acidului format alcool etilic:
CH2 = CH2 + H 2 O H +. t CH3-CH2-OH
alcool etilic este oxidat în prezența unui catalizator în acid acetic:
1 Această reacție este listat în carte. De fapt, reacția merge mai departe. Interacționează HCl și NH 3. NH3 + CI NSlNH 4 - produs de reacție final.
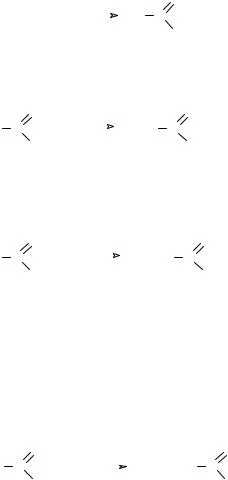
CH3-CH2 OH + O 2
În reacția acidului acetic cu acid cloroacetic cu clor se formează:
In tratarea acidului cloracetic cu amoniac sunt înlocuiți cu un atom de clor cu o grupare amino și acid acetic amino se formează:
Se aduce reacția Ecuații acid 2-aminopropionic: a) cu hidroxid de potasiu; b) cu acid sulfuric; c) cu etanol.
a) în reacția de hidroxid de potasiu cu acid 2-aminopropionic prezintă proprietăți acide:
b) prin reacția cu acid sulfuric, 2-aminopropionic prezintă proprietăți de bază:

c) Reacția alcoolului etilic cu esterul format:
substanță dată: a) etilamină: b) anilină; c) Acid aminoetanovaya. Cum se poate distinge între aceste substanțe? Scrieți ecuația reacțiilor corespunzătoare.
Acești agenți se pot distinge prin aspectul și proprietățile lor fizice. -etilamină - gaz cu un miros înțepător, care amintește de mirosul de amoniac este foarte solubil în apă. Anilină - odorant lichid nu este miscibil cu apa. Acid Aminoetanovaya - solid alb, ușor solubil în apă.
1) reacție adecvată cu apă:
CH3-CH2-NH2 + H2O [CH3-CH2-NH 3] + OH -
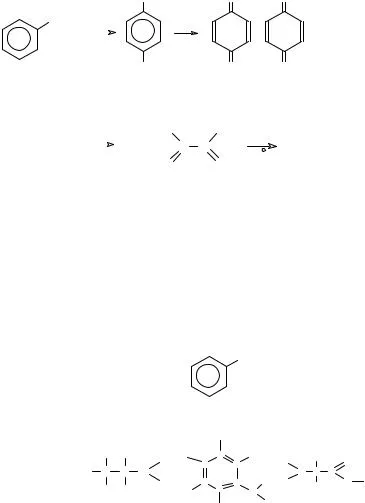
2) Aceste substanțe pot fi împărțite cu reacții de KMnO 4 soluție.
CH3-CH2-NH2 + KMnO 4
- nici o reacție
Fa un rezumat al răspunsului indicativ al etilamină, anilină și acid aminoetanovuyu (III, p. 22-23).
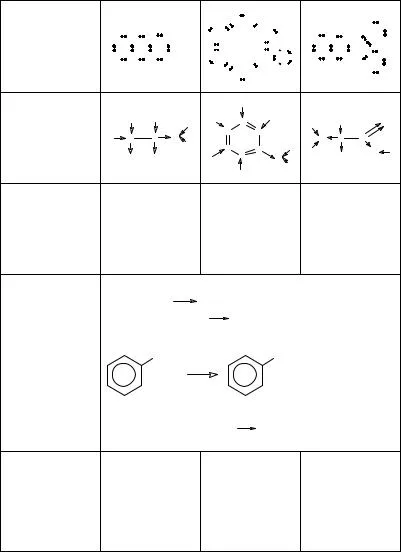
NH 3 ch3 I + NaOH
CH3 NH2 + NaI + H 2 O
c) Acid Aminoetanovaya:
CI-CH 2 -COOH + 2NH 3
amoniac, constituie un lyanistaya bine toxic
în apă; multe dintre
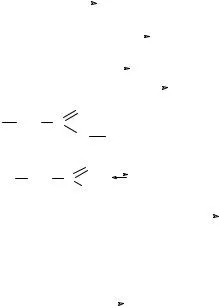
C 2 H 5 NH2 + CH3 CI -
C 2 H 5 NH2 + CH3 CI
1. NH2-CH2-COOH + KOH
COOH-CH2-NH2 + HCI
HOOC-CH2 NH3 + CI -
2. NH2-CH2-COOH + HOC 2 H 5
4. NH2-CH2-COOH + NH2-CH2-COOH
c) Acid Aminoetanovaya
NH2 CH2 COOH + KOH
NH2 CH2 COOK + H 2 O
Pentru sinteza Beltransgas
Cove în viață organică
Depresionară. de asemenea, utilizat
utilizat în me-
Folosind manualul de masă (p. 12-13), scrie ecuațiile de reacție ce caracterizează proprietățile chimice de bază: a) alcooli monohidroxilici saturați; b) fenoli; c) aldehide; d) limitarea acizilor carboxilici monobazici; d) esteri; e) amine; g) aminoacizi.

1) reacționează cu metalele active cu evoluție de hidrogen:
2CH 3 OH + 2Na = 2CH 3 ONa + H 2 ↑
2) oxidați la aldehide sau acizi carboxilici
4) Sub acțiunea halogenurilor de hidrogen sunt înlocuiți cu o grupare hidroxil cu un atom de halogen:
CH3-CH2-OH HCI + H 2 SO 4. t CH3-CH2-Cl + H 2 O
5) Atunci când este încălzit cu acid sulfuric concentrat, deshidratarea are loc, în funcție de temperatura eterilor produse sau alchene:
CH3-CH2-OH H 2 SO 4. 200 ° C CH2 = CH2 + H 2 O
2CH 3 CH 2 OH H 2 SO 4. 120 ° C CH3-CH2-CH2-CH3 + H 2 O
1) reacționează cu metalele active cu evoluția hidrogenului
și formarea de fenolații:
2) Ei reacționează cu alcalii pentru a forma fenolații:
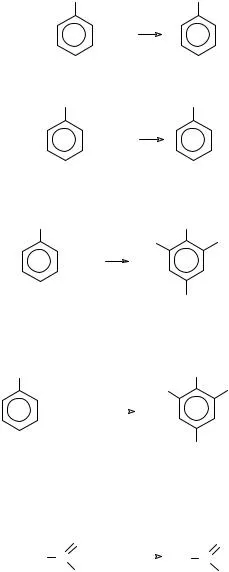
3) Atunci când acțiunea de substituție bromul are loc atomi de hidrogen de la brom inel de benzen:
4) Atunci când acțiunea acidului azotic sunt înlocuiți cu atomi de hidrogen din inelul benzenic la nitro:
1) este oxidat la acizi carboxilici, de exemplu, oxid de argint (I) sau hidroxid de cupru (II):

CH3 C + 2Cu (OH) 2
2) hidrogen pentru a forma alcooli sunt recuperate:
CH3 C + H 2 t, Cat CH3-CH2-OH
r) Limită de acid monobazic.
1) Într-o soluție apoasă disociază în ioni într-o mică măsură (ele sunt electroliții slabi):
CH3 COOH = CH3 COO - + H +
2) Ei reacționează cu metale, oxizi și hidroxizi metalici
pentru a forma săruri:
2CH 3 COOH + Mg = (CH3 COO) 2 Mg + H 2 ↑
2CH 3 COOH + CaO = (CH3COO) 2 Ca + H 2 O
2CH 3 COOH + Ca (OH) 2 = (CH3COO) 2 Ca + 2H 2 O
3) reacționează cu săruri ale acizilor slabi:
2CH 3 COOH + Na 2 CO 3 = SOONa 2CH 3 + CO 2 + H 2 O
4) reacționează cu alcooli, pentru a forma esteri: